 2021-06-01
2021-06-01 6665
6665
病理学家通常使用组织活检来诊断癌症,癌症扩散并测量治疗反应。同时,液体活检具有最小的侵入性,可以连续获得,并且可以在更早,更可治愈的阶段检测到癌症。对于改进的用于癌症检测的组织和液体活检工具,临床上尚未满足需求。
2020年8月13日,Ayuko Hoshino等人在Cell 在线发表题为“Extracellular Vesicle and Particle Biomarkers Define Multiple Human Cancers”的研究论文,该研究观察了来自组织外植体(TEs),血浆和其他体液的426个人类样品中细胞外囊泡和颗粒(EVP)的蛋白质组学特征。
在传统的外泌体标记中,CD9,HSPA8,ALIX和HSP90AB1代表泛EVP标记,而ACTB,MSN和RAP1B是新型泛EVP标记。为了确认EVP是理想的诊断工具,该研究分析了TE(n = 151)和血浆来源(n = 120)EVP的蛋白质组。TE EVP的比较可鉴定出以90%的敏感性/ 94%的特异性将肿瘤与正常组织区分开的蛋白质(例如VCAN,TNC和THBS2)。血浆来源的EVP(包括免疫球蛋白)的机器学习分类显示,在检测癌症时灵敏度为95%/特异性为90%。最后,该研究在TEs和血浆中定义了一组肿瘤类型特异性EVP蛋白,可以对未知原发性肿瘤进行分类。因此,EVP蛋白可以用作癌症检测和确定癌症类型的可靠生物标记。

病理学家通常使用组织活检来诊断癌症,癌症扩散并测量治疗反应。同时,液体活检具有最小的侵入性,可以连续获得,并且可以在更早,更可治愈的阶段检测到癌症。随着对液体活检技术用于早期癌症检测的期望的增长,外泌体可能会提供宝贵的资源。
外泌体是内体来源的30-150nm囊泡,富含核酸,脂质和蛋白质,可在正常的生理和病理学中介导细胞间的通讯。先前报道了肿瘤来源的外泌体蛋白在肿瘤进展,免疫调节和转移中的预后和功能重要性。此外,研究人员探讨了细胞外纳米颗粒的异质性,定义了三个不同的亚群,即小外泌体(Exo-S),大外泌体(Exo-L)和外泌体,统称为细胞外囊泡和颗粒(EVP)。
越来越多的证据表明,EVP可用于早期癌症检测,预后和指导治疗。EVP以> 10^9囊泡/ mL的浓度活跃地释放到周围循环中,为下游分析提供了充足的材料。基于质谱的蛋白质组分析已成为一种策略,可深入了解循环EVP的生物学和临床潜力。尽管有几种EVP蛋白质数据库公开可用,但关于EVP蛋白质组的知识仍然未知,包括:(1)用于可靠分离人中EVP的标记物,而与组织来源无关;(2)区分癌症与非癌症的标志物;(3)特定原发肿瘤(例如,肺,胰腺,乳腺等)特有的标志物。为了解决这一知识差距,该研究试图定义EVP蛋白特征,以区分癌症患者与健康个体。
为了鉴定通用的EVP标记并改善人类EVP的分离性,该研究通过蛋白质组分析对497个人类和鼠类样品进行了分析。在传统的外泌体标记中,71 kDa热休克相关的蛋白(HSPA8),热休克蛋白HSP 90-beta(HSP90AB1),CD9和程序性细胞死亡6相互作用蛋白(ALIX)是人类来源的EVP中最突出的标记。该研究确定了> 50%的人类样品共享的13种其他蛋白质,从而极大地扩展了人类EVP标记物的范围。
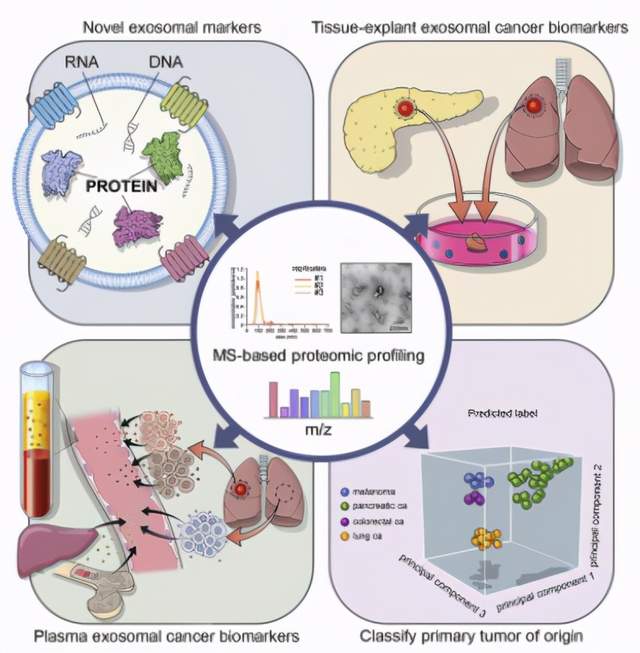
文章模式图(图源自Cell )
通过检查胰腺癌和肺癌患者可行手术标本中配对肿瘤和邻近组织的EVP蛋白质组,该研究确定了癌症特异性EVP蛋白特征。此外,通过比较匹配的组织外植体(TE)和血浆衍生的EVP,该研究发现癌症患者血浆中独特的肿瘤相关EVP蛋白,并确定EVP血浆蛋白源自肿瘤微环境,远处器官和免疫系统。
接下来,该研究分析了几种儿童和成人癌症的I–IV期癌症的组织和血浆EVP蛋白质组,并将它们与非肿瘤组织和健康对照(HC)血浆进行了比较。EVP蛋白质组的随机分类显示,癌症检测的特异性和敏感性分别为组织的90%和94%,血浆的95%和90%。重要的是,血浆衍生的EVP可以区分患者的癌症类型。这些数据表明,肿瘤相关的EVP蛋白可以作为早期癌症检测的生物标志物,并对不确定的原发肿瘤类型进行分类。
版权声明:本文转自“iNature”,文章转载只为学术传播,不代表本号观点,无商业用途,版权归原作者所有,如涉及侵权问题,请联系我们,我们将及时修改或删除。
 学术互动
学术互动

添加微信获取最新优惠、出版政策、课程直播信息,随时咨询客服/编辑,了解更多实时资讯



